带着4.74亿亏损IPO 纽脉医疗究竟有多“缺钱”?
扫一扫
分享文章到微信

扫一扫
关注99科技网微信公众号
原标题:带着4.74亿亏损IPO 纽脉医疗究竟有多“缺钱”?
最近,上海纽脉医疗科技股份有限公司二度向港交所递交招股书。
招股书显示,纽脉医疗是一家开发用于治疗结构性心脏病介入产品的中国心脏瓣膜器械公司。纽脉医疗已建立一套涵盖一款核心产品及八款其他瓣膜在研产品的全面产品组合,包括用于治疗人类心脏瓣膜的经导管置换及修复在研产品,以及七款介入式心脏手术的辅助器械。
而主流趋势二尖瓣反流(MR)是最为常见的瓣膜疾病,19年全球及中国中度及以上MR患者数分别达9670及1060万人。
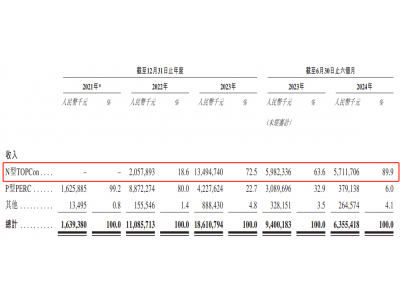
从市场规模来看,中国TAVR市场于2020年达到人民币5.56亿元,2017年至2020年的复合年增长率为138.0%,TAVR市场预计将于2025年增加至人民币50.56亿元。
于2030年增加至人民币114.91亿元,2020年至2025年的复合年增长率为55.5%,而2025年至2030年的复合年增长率为17.8%。
不过,在2022年的医疗市场上,竞争也格外的激烈。
今年2月,多家医疗公司港股招股书到期,其中包括北芯生命、推想医疗及美因基因。而美因基因在招股书失效后的第二天就更新申请文件,启动二次赴港IPO。
相对比美因基因,纽脉医疗似乎略逊一筹,截至目前,纽脉医疗产品并没有完成商业化。
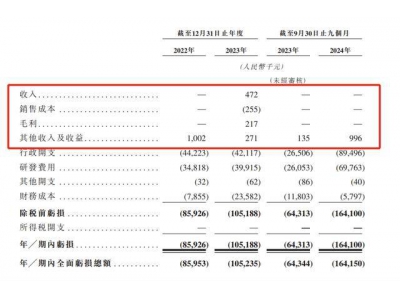
从财报数据来看,其并无通过销售在研产品产生任何收入,且亏损还在逐年扩大。截至2020年及2021年12月31日止年度,纽脉医疗的全面亏损总额分别为人民币1.15亿元及人民币4.74亿元。
一、渗透率仅0.46%的医疗新蓝海
不可否认的是,目前的心脏瓣膜器械市场,仍然处于研发前期。
近年来,在海外欧美等多个医工结合团队投巨资研发TMVR技术,但由于二尖瓣结构的复杂性与较高的技术壁垒,研发难度非常大,目前绝大多数均处于探索性或早期临床探索阶段。
在国内市场,虽然处于2021年同期,国内已有4家公司(德晋、捍宇、以心、佰仁)的5款TMV产品进入确证性临床阶段(3款修复及2款置换),亦有4家进入FIM试验阶段。
而二尖瓣介入修复器械(TMVr),最早是捍宇医疗核心产品ValveClamp,首次人体(FIM)临床试验,手术成功率达到100%,并于2019年2月启动了确证性临床试验。
不过,纽脉医疗的经心尖经导管二尖瓣置换术在研产品Mi-thos,却是首款在中国进入FIM临床试验的TMVR产品。

此外,根据弗若斯特沙利文的资料显示,纽脉医疗亦为中国少数同时掌握球扩式和自膨式技术的公司之一。
纽脉医疗已独立开发先进的介入式心脏瓣膜治疗技术平台,包含了在经导管瓣膜性器械开发及生产的所有方面属必要的全方位专有技术,尤其是自主克服了全球主流的球扩式技术的高技术门槛,掌握了该项技术。
事实上,截至最后实际可行日期,已有两家国际公司和四家国内公司的九项TAVR产品获得国家药监局批准,其中除了爱德华生命科学的SAPIEN 3以外,并无球扩式瓣膜产品。
而纽脉医疗的球扩式主动脉瓣在TAVR市场具有显著的差异化竞争优势,且其可应用于瓣中瓣治疗,也给广大有相关症状患者带来了实实在在的利益。
纽脉医疗的Mi-thos有希望成为国内首个获批的TMVR产品,在市场上具有一定的难替代性。

在产能方面,纽脉医疗在上海和成都拥用超过7600平方米的研发实验室、办公室及制造楼面空间,以及一座符合医疗器械生产质量管理规范的万级净化车间生产设施。
另据弗若斯特沙利文的资料,国家药监局已认可纽脉医疗的三项在研产品为获准进入加速特别审查的创新医疗器械。
这意味着,纽脉医疗成为中国所有经导管心脏瓣膜器械供应商中拥有最多项特别审查在研产品及在最广泛产品类别获得特别审查资格的厂家。

二、纽脉医疗的“压力增长指数”
有数据表明,二尖瓣反流作为临床中最为常见的心脏瓣膜疾病,在75岁以上的人群中,近10%的老年人患有中度以上二尖瓣反流,这个比例还有可能因老龄化而不断增加。
可以窥见的是,在未来的心脏瓣膜器械市场,随着相关技术和器械的进一步发展和医生经验的不断积累,TMV有望成为二尖瓣反流的主流治疗方式。
那么,能够做到创伤小、出血少、恢复快以及适用人群广等优势的二尖瓣反流方案,经导管二尖瓣修复术(TMVr)和经导管二尖瓣置换术(TMVR)也就成为了心脏瓣膜器械市场,竞争最激烈的研发产品。
从目前的纽脉医疗产品布局看,经导管二尖瓣修复术(TMVr)和经导管二尖瓣置换术(TMVR)正在同时推进的过程中。
但需要注意的是,在纽脉医疗TMVr与TMVR进入临床前,德晋医疗与捍宇医疗相对领先进入确证性临床,此外,捍宇医疗修复技术预计在2023年上市,这将会给纽脉医疗带来强大的冲击。
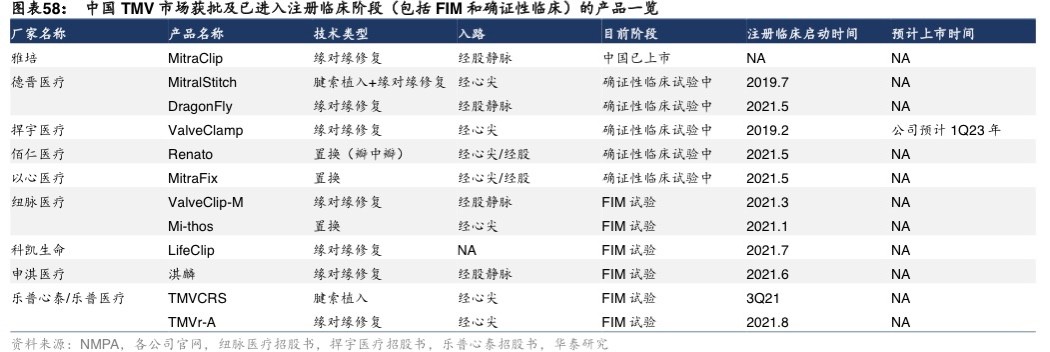
此外,相对比纽脉医疗的经导管二尖瓣置换术,佰仁医疗以及以心医疗的置换术已经到了确证性临床试验中。
在经导管二尖瓣置换术中,佰仁医疗针对置换中细分的瓣中瓣进行研发,显然更占优势。原因很简单,自体瓣中瓣患者占绝大多数,是现在TMVR的主要攻坚对象。
回到纽脉医疗上,即便TMVr与TMVR长期或是共存互补的关系,纽脉医疗同时布局介入二尖瓣修复及置换产品或有一定的协同效应,且长期销售天花板更高。
但无法忽略的是,TMVr目前应用最为成熟,但是存在适应症有限的问题,同时优先上市应用到市场上极其重要,为此,这对于TMVr停留在FIM试验阶段的纽脉医疗来说,上市进度更为迫切。
更重要的是,TMVR虽然在长期理念更加先进且适应症范围更广,但可能存在较多难点较难突破的瓶颈,未来仍需观察其疗效进展。

三、商业化盈利遥遥无期?
除了市场竞争外,纽脉医疗还面临着支出远远大于盈利的经营状态。
截至目前,纽脉医疗并无商业化的产品,且尚未从产品销售产生任何收入。2019年、2020年度以及截至2021年4月30日止四个月(2021年前4个月),纽脉医疗的净亏损分别为3073.1万元、1.15亿元及1.86亿元。
纽脉医疗的亏损绝大部分是由于研发开支、行政开支及融资成本所致。
2020年及2021年,纽脉医疗分别产生研发开支人民币7203.8万元及人民币3.07亿万元。纽脉医疗的研发开支自2020年至2021年增加,主要是由于研发人员的股份支付薪酬增加、研发人员人数增加及薪金增加、所用材料及耗材成本因研发阶段推进而增加等因素。

另外,纽脉医疗在本次IPO招股书中表示,IPO募集所得资金净额将主要用于核心和主要在研产品的研发、临床试验、注册备和商业化;产能开发;以及用于营运资金和一般公司用途。
诚然,根据TMV产品的研发周期以及高资金投入的特性不难看出,纽脉医疗在短时间内再次IPO的动机。
此外,心脏瓣膜器械市场的技术不断变革、新产品层出不穷及行业标准持续演变。
新产品的开发及商业化竞争激烈,纽脉医疗在医疗器械及相对成熟的心脏瓣膜器械市场面临来自全球主要医疗器械公司的竞争、招标及定价压力。
更值得注意的是,目前国内TMV市场只有雅培的MitraClip单个产品获批,根据湖南及广西招采网,MitraClip最新终端中标价约35万元/套。
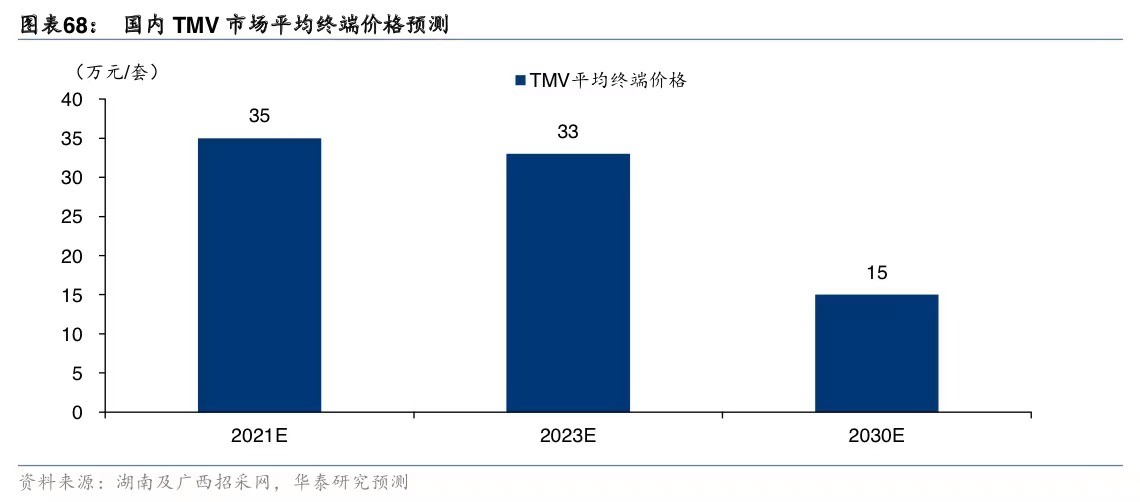
参考TAVR领域的定价情况,预计国产TMV产品初始定价有望在20-30万元/套,随着销量提升及竞争加剧,价格预计逐渐下降。
最终预计国内TMV市场平均终端价格有望从2021年的35万元/套降低至2023年的33万元/套,并预计最终降低至2030年的15万元/套。
诚然,在国产占比逐渐提升,且国产价格预计随着竞争加剧逐渐下降的态势下,纽脉医疗想要提升产品利润率,或许将变得更加艰难。
在港交所修改《上市规则》引入18A章,允许未盈利生物科技公司到中国香港上市的友好条件下,或许真的能够让医疗企业快速发展起来,但行业间的竞争依然“如影随形”。
投稿邮箱:jiujiukejiwang@163.com 详情访问99科技网:http://www.fun99.cn